
Cómo se calculan los átomos
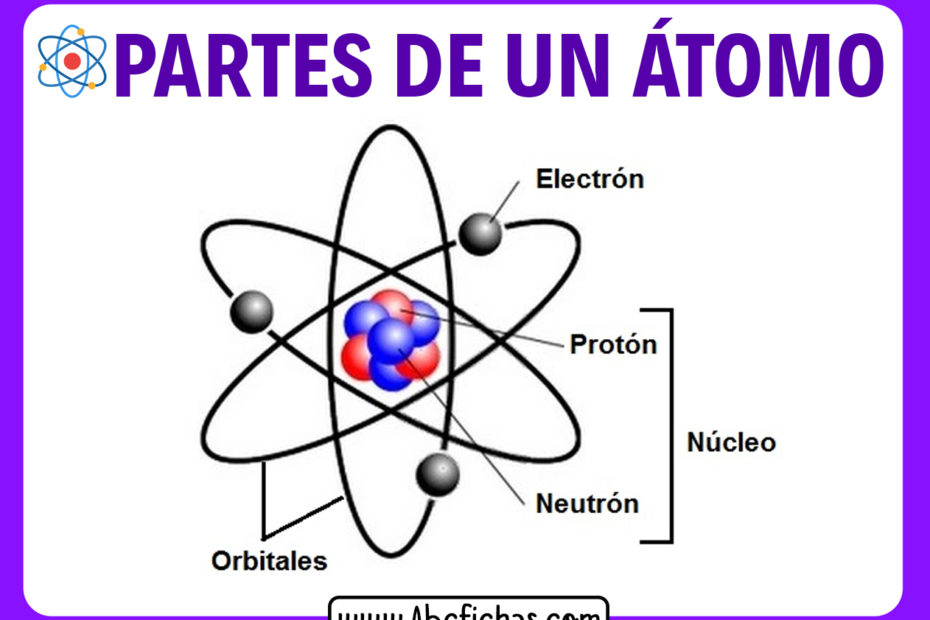
Cuando se trata de calcular el número de átomos en atomo muestra, es importante entender los conceptos básicos de la química y la estructura atómica. Los átomos son las unidades más pequeñas de la materia y están compuestos por partículas subatómicas como protones, neutrones y electrones. Aquí te presentamos la forma de calcular estos diminutos componentes:
1.
Conocer la fórmula química
El primer paso para calcular el número de átomos en una muestra es conocer la fórmula calcual del compuesto. La fórmula especifica los tipos y la cantidad de átomos presentes en la molécula.
2.
Determinar los coeficientes estequiométricos
Los coeficientes estequiométricos en la fórmula química nos indican la proporción en la que los átomos están presentes en el compuesto.
Estos coeficientes se obtienen mediante el balanceo de la ecuación química del compuesto.
3. Utilizar la constante de Avogadro
La constante de Avogadro, que es aproximadamente igual a 6.022 x 10^23, indica la cantidad de partículas (átomos, moléculas, electrones, etc.) contenidas en un mol de cualquier sustancia.

Utilizando esta constante, podemos determinar el número de átomos.
4. Aplicar las relaciones estequiométricas
Usando los coeficientes estequiométricos de la fórmula química y la constante de Avogadro, podemos establecer una relación entre los átomos atmos en la muestra y el número de átomos en un mol.
Multiplicando los coeficientes estequiométricos por la constante de Avogadro, obtenemos el número de átomos en la muestra.
5. Calcular el número de átomos
Finalmente, multiplicamos el número de moles del compuesto por el número de átomos en un mol para obtener el número total de átomos en la muestra.
Es importante recordar que este método solo nos brinda la cantidad total de átomos en una muestra, y no nos dice nada sobre su distribución o ubicación dentro de la misma.
¡Ahora que conoces cómo se calculan los átomos, puedes aplicar este Clmo para explorar más a fondo el mundo de la química y comprender mejor la estructura de la materia!








